Bazơ là gì ? Bazơ sẽ có những tính chất vật lí, tính chất hóa học? Bazơ sẽ được ứng dụng như thế nào trong cuộc sống? Để biết rõ hơn về Bazơ hãy cùng với chúng tôi đi tìm hiểu trong bài viết sau đây nhé.
Xem thêm:

Bazơ là gì ?
– Bazơ là hợp chất hóa học mà phân tử bao gồm có một nguyên tử kim loại liên kết với một hay nhiều nhóm OH (Hydroxit), trong đó hóa trị của kim loại bằng số nhóm Hydroxit.
Một định nghĩa khác, Bazơ là những chất hòa tan trong nước và có độ pH > 7 khi ở trong dung dịch.
Công thức của Bazơ
– Bazơ có công thức hóa học tổng quát sau đây:
M(OH) n
=> Trong đó:
- M là môt kim loại
- n là Hóa trị của kim loại.
Ví dụ :
- CTHH của bazơ Natrihidroxit là NaOH
- CTHH của bazơ Sắt (III) hidroxit là H2CO3
- CTHH của bazơ kali hidroxit là KOH
Tính chất vật lí của bazơ
Sau đây là những tính chất vật lý nổi bật của bazơ:
- Bazơ có tính nhờn như xà phòng.
- Chúng có mùi và có vị đắng.
- Khi chúng ở nồng độ cao có tính ăn mòn chất hữu cơ và tác dụng mạnh với các hợp chất axit.
- Bazơ kiềm có độ pH > 7.
- Chúng tồn tại ở dạng rắn, bột, đôi khi là ở trạng thái dung dịch.
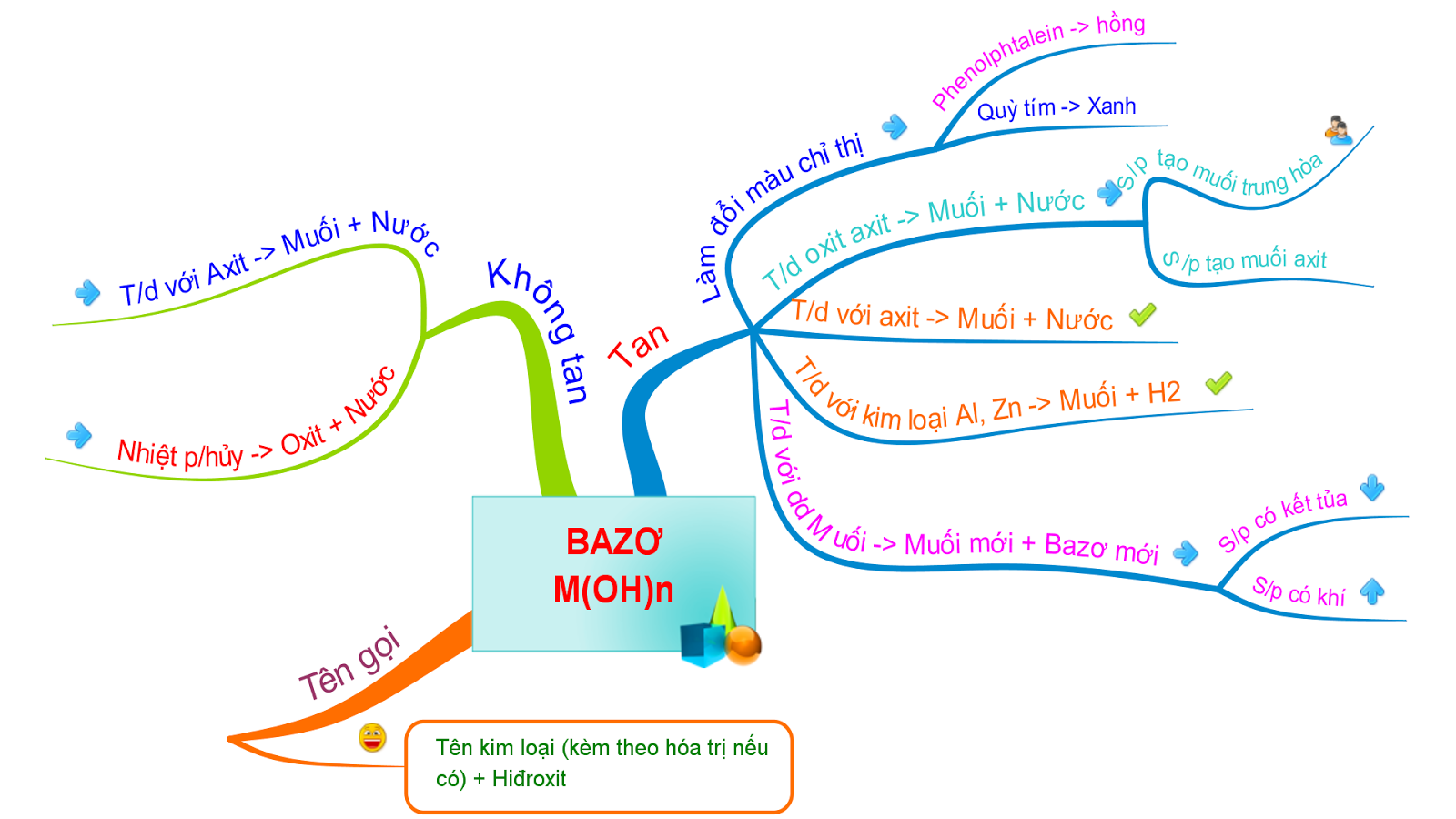
Tính chất hóa học của bazơ
Làm đổi màu giấy quỳ tím, dung dịch phenolphthalein
– Khi nhỏ một vài giọt dung dịch bazo (NaOH) vào giấy quỳ tím. Sau đó tiến hành quan sát sự biến đổi, ta thấy màu quỳ tím chuyển sang màu xanh.
– Từ đó kết luận rằng, dung dịch bazơ làm đổi màu giấy quỳ tím thành xanh. Dựa vào đặc điểm này, ta có thể dùng giấy quỳ tím để giúp nhận biết dung dịch bazơ.
– Bên cạnh đó, bazơ còn làm dung dịch phenolphthalein từ không màu đổi sang màu đỏ.
Bazơ tác dụng với oxit axit tạo thành muối và nước
Theo phương trình phản ứng như sau:
2NaOH + SO2 → Na2SO3 + H2O
3Ca(OH)2 + P2O5 → Ca3(PO4)2↓ + 3H2O
Bazơ tác dụng với axit tạo thành muối và nước
Phương trình phản ứng:
KOH + HCl → KCl + H2O
Cu(OH)2 + 2HNO3 → Cu(NO3)2 + H2O
Bazo tác dụng với muối tạo thành muối mới và bazơ mới
Phương trình phản ứng:
2NaOH + CuSO4 → Na2SO4 + Cu(OH)2↓
Bazơ (không tan) bị nhiệt phân hủy thành oxit và nước
Phương trình phản ứng:
Cu(OH)2 → CuO + H2O.
2Fe(OH)3 →Fe2O3 + 3H2O
Ứng dụng của Bazơ
Dùng để xử lý nước (đặc biệt là nước hồ bơi)
– Khi hòa tan trong nước, Bazơ có khả năng làm tăng nồng độ pH. Ngoài ra người ta cũng dùng nó để trung hòa và khử cặn bẩn trong đường ống cấp nước.
Trong ngành công nghiệp hóa chất, dược
– Bazơ được sử dụng để sản xuất sản phẩm có chứa gốc Sodium như Sodium phenolate (thuốc Aspirin), Sodium hypochlorite (Javen),… làm chất tẩy trắng, chất khử trùng. Ngoài ra, nó còn được dùng làm nước rửa chén nhờ khả năng thủy phân chất béo trong dầu mỡ động vật.
– Được sử dụng làm hóa chất để xử lý đối với gỗ, tre, nứa,… để làm nguyên liệu sản xuất giấy dựa theo phương pháp Sunphat và Soda.
Trong ngành công nghiệp dệt, nhuộm
– Nhiều bazơ được dùng để làm chất phân hủy pectins, sáp trong khâu xử lý vải thô, làm cho vải dễ hấp thụ màu nhuộm và có độ bóng.
Trong ngành dầu khí
– Bazơ dùng để cân bằng độ pH cho dung dịch khoan, như là loại bỏ sulphur, các hợp chất sulphur hay các hợp chất axit có trong tinh chế dầu mỏ.
– Được dùng để pha chế dung dịch kiềm giúp xử lý rau
Trong ngành thực phẩm
– Được dùng để pha chế dung dịch kiềm giúp xử lý rau, hoa quả trước khi chế biến hoặc đóng hộp chúng.
Trong phòng thí nghiệm
– Bazơ là một hóa chất vô cùng quan trọng, được dùng để phục vụ trong học tập và nghiên cứu.