Axit Cacbonic (H2CO3) là gì? Bạn có muốn tìm hiểu về chất này hay không? Trong bài viết sau đây chúng tôi sẽ mang đến cho bạn những kiến thức quan trọng về Axit Cacbonic (H2CO3) này nhé.
Xem ngay:
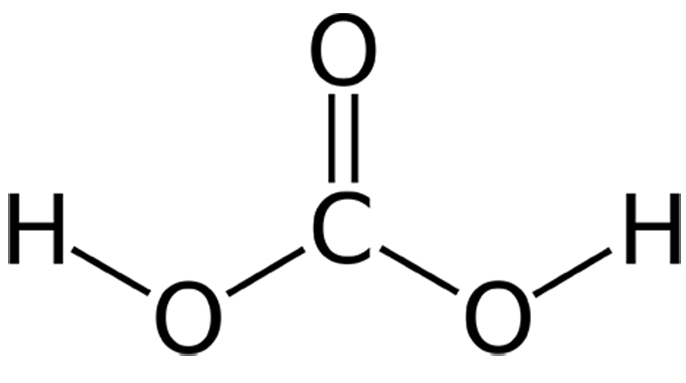
Axit Cacbonic (H2CO3) là gì?
Trạng thái tự nhiên và tính chất vật lý của axit cacbonic
- Khí CO2 hòa tan trong nước mưa và nước tự nhiên: khoảng 90 cm3 khí CO2 hòa tan được trong 1000 cm3 nước.
- Một phần khí CO2 tác dụng với nước tạo thành dung dịch axit cacbonic. Phần lớn khí CO2 còn lại vẫn tồn tại trong khí quyển.
Tính chất hóa học của axit cacbonic
- Axit cacbonic là một axit yếu: nó làm đổi màu quỳ tím thành đỏ nhạt.
- Axit cacbonic là một axit kém bền: H2CO3 tạo thành trong các phản ứng hóa học dễ bị phân hủy ngay thành khí CO2 và nước.
Muối Cacbonat
Phân loại muối cacbonat
– Có 2 loại muối cacbonat: Cacbonat trung hòa và Cacbonat axit
- Muối Cacbonat trung hoà là muối cacbonat không còn nguyên tố H trong thành phần gốc axit.
Ví dụ: Canxi Cacbonat CaCO3; Natri Cacbonat Na2CO3; Magie Cacbonat MgCO3;…
- Muối Cacbonat axit là muối hyđrocacbonat có nguyên tố H trong thành phần gốc axit.
Ví dụ: Canxi Hidrocacbonat Ca(HCO3)2; Kali hidrocacbonat KHCO3;…
Tính chất của muối cacbonat
Tính tan
- Đa số các muối cacbonat đều không tan trong nước, trừ một số muối cacbonat của kim loại kiềm: Na2CO3, K2CO3…
- Hầu hết các muối hiđrocacbonat đều tan trong nước: Ca(HCO3)2, Mg(HCO3)2…
Tính chất hóa học
Tác dụng với axit:
– Muối cacbonat tác dụng với axit tạo thành muối mới và giải phóng khí CO2.
Na2CO3 + 2HCl → 2NaCl + CO2 + H2O
NaHCO3 + HCl → NaCl + CO2 + H2O
Tác dụng với dung dịch bazơ:
– Một số muối cacbonat tác dụng với dung dịch bazơ tạo thành tạo thành muối cacbonat không tan và bazơ mới.
Na2CO3 + Ba(OH)2 → BaCO3 ↓ + 2NaOH
K2CO3 + Ca(OH)2 → CaCO3 ↓ + 2KOH
– Muối hiđrocacbonat tác dụng với dung dịch kiềm tạo thành muối trung hòa và nước.
KHCO3 + KOH → K2CO3 + H2O
NaHCO3 + NaOH → Na2CO3 + H2O
Tác dụng với dung dịch muối:
– Dung dịch muối cacbonat có thể tác dụng với một số dung dịch muối tạo thành 2 muối mới.
Na2CO3 + BaCl2 → BaCO3 ↓ + 2NaCl
K2CO3 + Mg(NO3)2 → MgCO3 ↓ + 2KNO3
Muối cacbonat bị nhiệt phân hủy:
– Nhiều muối cacbonat (trừ muối cacbonat của kim loại kiềm như Na2CO3, K2CO3…) bị nhiệt phân hủy giải phóng khí CO2.
CaCO3 (t°) → CaO + CO2
2NaHCO3 (t°) → Na2CO3 + CO2 + H2O
Chu trình của cacbon trong tự nhiên
– Trong tự nhiên luôn có sự chuyển hoá cacbon từ dạng này sang dạng khác. Sự chuyển hoá này diễn ra thường xuyên, liên tục và tạo thành chu trình khép kín.
Ứng dụng của muối cacbonat
- CaCO3: Thành phần chính của đá vôi, đá phấn được dùng làm nguyên liệu sản xuất xi măng, vôi…
- Na2CO3: Dùng để sản xuất thủy tinh, nấu xà phòng…
- NaHCO3: Dùng để sản xuất dược phẩm, hóa chất trong bình cứu hỏa…