Axit sunfuric (H2SO4) là gì? Để hiểu hơn về Axit sunfuric (H2SO4) và có thể áp dụng một cách triệt để nhất hãy theo dõi nội dung ngay sau đây để biết thêm thông tin chi tiết nhé.
Tham khảo:
Axit sunfuric (H2SO4) là gì?
– Axit Sunfuric là tên gọi chính của hóa chất H2SO4, tên gọi này được bắt nguồn từ tiếng Pháp là acide sunfurique.
– Axit Sunfuric là một axit vô cơ gồm các nguyên tố lưu huỳnh, oxy, hidro. Tồn tại ở dạng chất lỏng sánh như dầu, không mùi, không màu, không bay hơi, nặng gấp 2 lần nước (H2SO4 98% có D = 1,84g/cm3). H2SO4 có khả năng tan hoàn toàn trong nước theo bất kể tỷ lệ nào, khi tan trong nước Axit Sunfuric tỏa rất nhiều nhiệt.
– Trên thế giới, không tìm thấy được H2SO4 nguyên chất tinh khiết, bởi áp lực rất lớn giữa nước và axit sunfuric. Ngoài ra, hợp chất H2SO4 còn là thành phần của mưa axit.
– Nguyên nhân là do sự gia tăng SO2 và NO2 trong khí quyển, trong quá trình mưa, dưới tác dụng của bức xạ môi trường. Các oxit này sẽ tác dụng với hơi nước trong khí quyển để hình thành Axit H2SO4 và một số axit khác như (Axit nitric, Axit sunfuro) gây lên hiện tượng mưa axit.
– Axit Sunfuric có công thức phần tử là H2SO4.
Tính chất vật lí
- H2SO4 là chất lỏng không màu, dạng sánh hơi nhớt, nặng hơn nước, khó bay hơi, tan vô hạn trong nước.
- H2SO4 đặc hút mạnh nước và tỏa rất nhiều nhiệt, do đó trong quá trình pha loãng, nên đổ axit từ từ vào nước (không làm ngược lại), bởi H2SO4 sẽ gây bỏng.
- H2SO4 có thể làm than hóa các hợp chất hữu cơ.
Tính chất hóa học
Đối với Axit sunfuric loãng
H2SO4 là một axit mạnh, kể cả với nồng độ loãng thì hóa chất này cũng mang đầy đủ tính chất hóa học của một axit như:
- Axit Sunfuric làm chuyển màu quỳ tím thành đỏ
- H2SO4 phản ứng với các kim loại đứng trước Hidro (trừ Pb) tạo muối sunfat
Phương trình hóa học minh họa:
2Al + 3H2SO4loãng → Al2(SO4)3 + 3H2↑
– H2SO4 phản ứng với oxit bazơ tạo muối mới (trong muối kim loại giữ nguyên giá trị) và nước
Phương trình hóa học minh họa:
AlO + H2SO4loãng → AlSO4 + H2O
– H2SO4 phản ứng với bazo tạo nước và muối mới:
Phương trình hóa học minh họa:
NaOH + H2SO4loãng → NaHSO4 + H2O
2NaOH + H2SO4 → Na2SO4
– H2SO4 phản ứng với muối tạo muối mới và axit mới
Phương trình hóa học minh họa:
Na2CO3 +H2SO4loãng → Na2SO4 + H2O + CO2
Đối với Axit sunfuric đặc
H2SO4 đặc là hợp chất có axit và oxi hóa rất mạnh. Được chứng minh qua các thí nghiệm sau:
– Thí nghiệm tác dụng với kim loại: Cho Axit Sunfuric đặc tác dụng với mảnh kim loại Cu tạo dung dịch màu xanh và có khí bay ra, có mùi sốc.
Phương trình hóa học:
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
– Thí nghiệm tác dụng với phi kim: Cho H2SO4 đặc tác dụng với nguyên tố phi kim như Cacbon (C) và Lưu Huỳnh (S) tạo thành oxit phi kim và nước, giải phóng khí SO2
Phương trình hóa học:
S + 2H2SO4 → 3SO2↑ + 2H2O
C + 2H2SO4 → CO2 + 2H2O + 2SO2↑
– Axit Sulfuric tác dụng với các chất khử khác: Cho H2SO4 tác dụng với chất khử (FeO, FeSO4) tạo thành muối và nước, giải phóng khí SO2
Phương trình hóa học:
2FeO + 4H2SO4 → Fe2(SO4)3 + SO2↑ + 4H2O
2FeSO4 + 2H2SO4 → Fe2(SO4)3 + SO2↑ + 2H2O
– Thí nghiệm tính háo nước của Axit Sunfuric: Cho H2SO4 vào cốc đựng đường, sau phản ứng đường trong cốc chuyển màu đen và sôi trào
Phương trình hóa học:
C12H22O11 + H2SO4 → 12C + H2SO4.11H2O
Axit sunfuric tồn tại ở mấy dạng?
Tùy vào mục đích sử dụng mà hợp chất Axit Sunfuric tồn tại ở nhiều dạng khác nhau. Cụ thể như:
- 98% là tồn tại ở dạng axit đậm đặc
- H2SO4 loãng sử dụng trong phòng thí nghiệm thường chỉ có 10%.
- Sử dụng cho ắc quy khoảng 33,5%
- 77,67% được dùng trong tháp sản xuất hay axit glover
- Hàm lượng 62,18% là axit được dùng để sản xuất phân bón
Tính dẫn điện và tính phân cực
– Axit sunfuric khan là một chất lỏng phân cực, hằng số điện môi khoảng 100. Điều này là do nó có thể phân ly bằng cách tự proton hóa chính nó, là một quá trình được biết đến là tự proton hóa.
Phương trình thể hiện:
2 H2SO4 → H3SO4+ + HSO4‾
Ứng dụng của H2SO4 trong cuộc sống
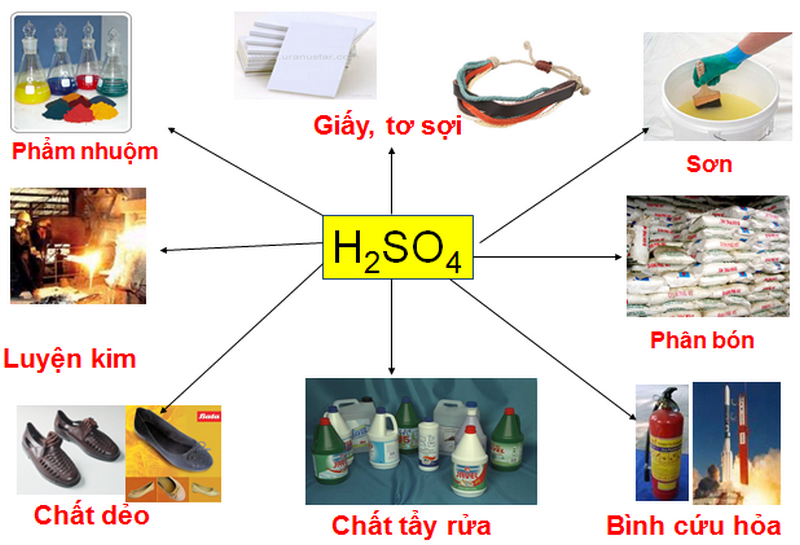
Trong sản xuất phân bón
– Axit sunfuric chủ yếu được sử dụng trong sản xuất axit photphoric, là chất được sử dụng để sản xuất các loại phân photphat, và cũng dùng để sản xuất Amoni sunfat.
Trong sản xuất công nghiệp
– Axit sunfuric được sử dụng rộng rãi trong quá trình sản xuất kim loại như sản xuất đồng, kẽm và dùng trong làm sạch bề mặt thép và dung dịch tẩy gỉ.
– Axit sunfuric còn được sử dụng để sản xuất nhôm sunfat (ví dụ như phèn làm giấy). Sản xuất các loại muối sunfat, tẩy rửa kim loại trước khi mạ, chế tạo thuốc nổ, chất dẻo, thuốc nhuộm, sản xuất dược phẩm.
– Hỗn hợp axit với nước được dùng để làm chất điện giải trong hàng loạt các dạng ắc quy, axit chì…
– Mỗi năm có khoảng 160 triệu tấn H2SO4, trong đó nổi bật khi được sử dụng trong các ngành sản xuất như phân bón 30%, luyện kim 2%, phẩm nhuộm 2%, chất dẻo 5%, chất tẩy rửa 14%, giấy, sợi 8%…
Trong xử lý nước thải
– Sản xuất nhôm hidroxit là chất được sử dụng trong các nhà máy xử lý nước để lọc các tạp chất, cũng như cải thiện mùi vị của nước, trung hòa pH trong nước, và sử dụng để loại bỏ các ion Mg2+, Ca2+ có trong nước thải
Lưu ý: Về tác hại của axit sunfuric, đây là hóa chất nguy hiểm, hạng một ăn mòn và gây bỏng rộp da. Vì thế khi sử dụng nên trang bị đầy đủ các dụng cụ chuyên dụng, mặt nạ phòng độc cá nhân, khẩu trang, tủ hút khio pha chế…
Trong phòng thí nghiệm
– Axit sunfuric là hợp chất đậm đặc dùng để điều chế các axít khác yếu hơn: HNO3. HCl ở trong thí nghiệm.
– Là hóa chất không thể thiếu trong các phản ứng để đưa ra những kết quả, ứng dụng vào trong các lĩnh vực khác của cuộc sống.
Lưu ý khi sử dụng H2SO4
- Đeo găng tay dày dặn, đạt chuẩn.
- Mặc đầy đủ quần áo bảo hộ khi tiếp xúc với hóa chất.
- Khi sử dụng đeo kính và mũ đầy đủ.
- Không đi dép hay chân đất nên đi giày bảo hộ hoặc ủng.
- Tuyệt đối không xử lý nó trên một băng ghế mở.
- Tuyệt đối không đổ nó khỏi chai chứa.
- Tuyệt đối không pipette ra với miệng.
- Phải dùng pipet thủy tinh dày với nút cao su.
- Tuân theo đúng chỉ dẫn trên nhãn sản phẩm.
- Tuyệt đối không đổ nước thẳng vào chai chứa để tẩy rửa.
- Khi pha loãng H2SO4, tuyệt đối không được đổ nước vào axit mà cần đổ từ từ axit vào nước.
- Khi đun nóng H2SO4 sẽ giải phóng ra chất SO2 và SO3, đây là những loại khí rất độc hại, có thể cần trang bị mặt nạ phòng độc nếu đun nóng axit với số lượng lớn.
Lưu ý khi bảo quản
- Lưu trữ axit bằng bồn nhựa, phuy nhựa.
- Không dùng các thùng kim loại để đựng, bởi tính axit mạnh sẽ làm oxy hóa ăn mòn kim loại.
- Đậy nắp thật kín đáo, để nơi khô ráo, thoáng mát, tránh ánh nắng trực tiếp.
- Không để gần nơi chứa bazơ hay chất khử.
- Tránh bảo quản chung với các kim loại nặng, kim loại nhẹ, các chất có tính axit như HCl, Axit Nitric gây cháy nổ, rất nguy hiểm.